Odpowiedź:
Przykłady poprawnych odpowiedzi
Szukane:
V NO2
Dane:
m Cu = 0,48 g
M Cu = 64 g·mol–1
Objętość molowa gazu w warunkach normalnych
V mol = 22,4 dm3 ·mol–1
Rozwiązanie:
I sposób:
1 mol Cu — 2 mole NO2 i MCu = 64 g·mol –1 i Vmol = 22,4 dm3 ·mol–1
⇓
64 g Cu — 2 · 22,4 dm3 = 44,8 dm3 NO2
0,48 g Cu — x NO2
x = 336 cm3
II sposób:
Z równania reakcji:
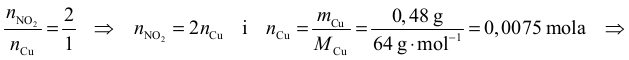
nNO2 = 2 ⋅ 0,0075 mola = 0,015 mola
VNO2 = nNO2 Vmol = 0,015 mola ⋅ 22, 4 dm3 ⋅ mol−1 = 0,336 dm3 = 336 cm3
Odpowiedź:
W czasie opisanej reakcji wydzieliło się 336 cm3 (w przeliczeniu na warunki normalne) gazu.