Odpowiedź:
Przykład poprawnej odpowiedzi
Dane:
VN2 = Vpoduszki= 12 dm3
mNaN3 = 13,00 g
t = 22,00 ºC → T = (273,15 + 22,00) K = 295,15 K
MNaN3 = MNa+ 3 MN = (23 + 3·14) g · mol–1 = 65 g · mol–1
R = 83,1 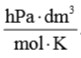
Szukane:
p
Rozwiązanie:
Obliczenie liczby moli azotu:
Z równania reakcji 2NaN3 → 2Na + 3N2:
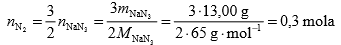
Obliczenie ciśnienia w poduszce:
pV = nRT ⇒
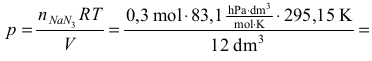
p = 613,17 hPa ≈ 613 hPa
Odpowiedź: Ciśnienie panujące w poduszce powietrznej: 613 hPa.