Odpowiedź:
Przykłady poprawnych odpowiedzi
Dane:
cp1 = 10,00%
cp2 = 6,00%
d1= 1,0121 g · cm−3
d2= 1,0066 g · cm−3
mr1 = 200 g
Szukane:
cm1, cm2
Rozwiązanie:
I sposób
Stężenie molowe roztworu kwasu octowego o stężeniu procentowym 10%
M CH3COOH = 60 g · mol −1
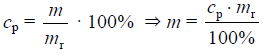
mr = d · Vr
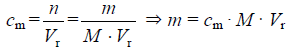
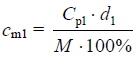
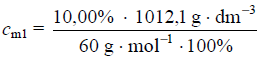
cm1 = 1,687 mol · dm−3
Stężenie molowe roztworu kwasu octowego o stężeniu procentowym 6,00%
M CH3COOH = 60 g · mol −1
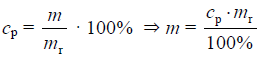
mr = d · Vr
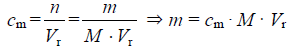
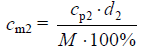
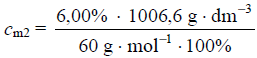
cm = 1,007 mol · dm−3
II sposób
Stężenie molowe roztworu kwasu octowego o stężeniu procentowym 10,00%
M CH3COOH = 60 g · mol −1
ms = 20 g
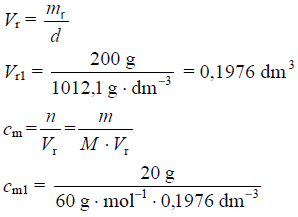
cm1 = 1,687 mol · dm−3
Stężenie molowe roztworu kwasu octowego o stężeniu procentowym 6,00%
M CH3COOH = 60 g · mol −1
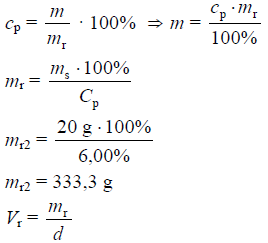
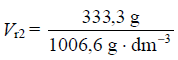
Vr2 = 0,331 dm3
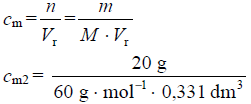
cm2 = 1,007 mol · dm−3
Odpowiedź: Stężenie molowe roztworu kwasu octowego o stężeniu procentowym 10,00% wynosi