Odpowiedź:
Np.:
objętość H2 (wydajność 100%) = 3 ∙ 2 m3 = 6,0 m3
objętość CO (wydajność 100%) = 2 m3
objętość H2 (wydajność 100%) = 1,6 m3
22,4 dm3 CH4 – 3 · 22,4 dm3 H2
200 dm3 – x dm3
160 dm3 CO ⇒ 160 dm3 H2
160 dm3 H2 – 100%
x4 dm3 – 60%
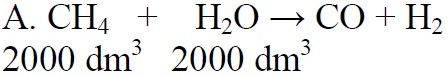
B. 3CO + 3H2O →3CO2 + 3H2
2000 dm3 – 100%
x – 60%
4800,77 dm3 + 1200 dm3 = 6001 dm3 = 6 m3
Obliczenie objętości wodoru powstającego w reakcji A:
CH4 + H2O → CO + 3H2
objętość H2 (wydajność 80%) = 80% z 6 m3 = 4,8 m3
Obliczenie objętości tlenku węgla(II) powstającego w reakcji A:
objętość CO (wydajność 80%) = 80% z 2 m3 = 1,6 m3
Obliczenie objętości wodoru powstającego w reakcji B:
CO + H2O → CO2 + H2
objętość H2 (wydajność 60%) = 60% z 1,6 m3 = 0,96 m3
Obliczenie całkowitej objętości wodoru:
objętość H2 (całkowita) = 4,8 m3 + 0,96 m3 = 5,76 m3 ≈ 6 m3 lub 6
Przykładowe ocenione odpowiedzi
CH4 + H2O → CO + 3H2
22,4 dm3 CH4 – 3 · 22,4 dm3 H2
200 dm3 – x dm3
x = 600 dm3 H2
600 dm3 H2 – 100%
x1 dm3 – 80%
x1 dm3 – 80%
x1= 480 dm3 H2
22,4 dm3 CH4 – 22,4 dm3 CO
200 dm3 – x2 dm3
200 dm3 – x2 dm3
x2 = 200 dm3 CO
200 dm3 CO – 100%
x3 dm3 – 80%
x3 dm3 – 80%
x3= 160 dm3 CO
CO + H2O → CO2 + H2
160 dm3 CO ⇒ 160 dm3 H2
160 dm3 H2 – 100%
x4 dm3 – 60%
x4= 96 dm3 H2
Vc= 480 + 96 = 576 dm3 = 6 m3
1 pkt – zastosowano poprawną metodę obliczenia, ale popełniono błędy w przeliczaniu jednostek.
22,4 dm3 – 1 mol
2000 dm3 – x moli
2000 dm3 – x moli
x = 89,3 mola
1 mol CH4 – 3 mole H2
89,3 mola CH4 – x moli H2
x = 267,9 mola
89,3 mola CH4 – x moli H2
x = 267,9 mola
267,9 mola H2 – 100%
x – 80%
x = 214,32 mola
x – 80%
x = 214,32 mola
1 mol – 22,4 dm3
214,32 mola – x dm3
x = 4800,77 dm3
214,32 mola – x dm3
x = 4800,77 dm3
B. 3CO + 3H2O →3CO2 + 3H2
VH2 = 2000 dm3
2000 dm3 – 100%
x – 60%
x = 1200 dm3
4800,77 dm3 + 1200 dm3 = 6001 dm3 = 6 m3
0 pkt – zastosowano błędną metodę obliczenia.
schemat punktacji
2 pkt – poprawna metoda, poprawne obliczenia oraz podanie wyniku z wymaganą dokładnością.
1 pkt – poprawna metoda obliczenia i popełnienie błędów rachunkowych lub podanie wyniku z niewłaściwą dokładnością.
0 pkt – niepoprawne obliczenia wynikające z zastosowania błędnej metody lub brak rozwiązania.
1 pkt – poprawna metoda obliczenia i popełnienie błędów rachunkowych lub podanie wyniku z niewłaściwą dokładnością.
0 pkt – niepoprawne obliczenia wynikające z zastosowania błędnej metody lub brak rozwiązania.