Odpowiedź:
Np.:
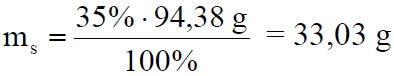
MHNO3 = 1,01 g · mol-1 + 14,01 g · mol-1 + 3 · 16,00 g · mol-1 = 63,02 g · mol-1
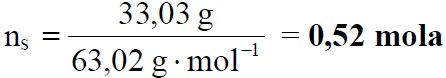
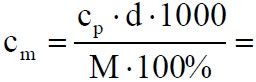
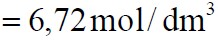
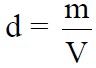
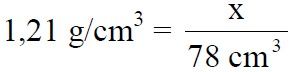
0 pkt – zastosowanie błędnej metody obliczenia (ocena i uzasadnienie są niezgodne z obliczeniami, mimo że są zgodne z opisem wyników doświadczenia umieszczonym w informacji do zadania).
kwas (HNO3) i zasada (KOH) reagują w stosunku molowym 1 : 1
obliczenie masy roztworu HNO3
mr = 78,00 cm3 · 1,21 g · cm-3 = 94,38 g
obliczenie masy substancji (HNO3)
Masa molowa HNO3
MHNO3 = 1,01 g · mol-1 + 14,01 g · mol-1 + 3 · 16,00 g · mol-1 = 63,02 g · mol-1
obliczenie liczby moli HNO3
obliczenie liczby moli KOH
nKOH = 2,00 mol · dm-3 · 0,25 dm3 = 0,50 mola
i porównanie liczby moli
i porównanie liczby moli
Hipoteza nie była poprawna. Odczyn roztworu nie jest obojętny
ponieważ w roztworze znajdują się kationy wodorowe pochodzące
z dysocjacji nadmiaru kwasu azotowego(V). Fenoloftaleina nie pozwala
na jednoznaczne określenie, czy roztwór ma odczyn obojętny, słabo
zasadowy, czy kwasowy.
Przykładowe ocenione odpowiedzi
78 cm3 = 0,078 dm3
cm = 6,72 mol/dm3
n = 0,52 mola
250 cm3 = 0,25 dm3
n = 0,52 mola
250 cm3 = 0,25 dm3
cm = 2 mol/dm3
n = 0,5 mola
n = 0,5 mola
Hipoteza była poprawna. Odczyn roztworu jest obojętny, ponieważ znajduje się w nim tyle samo jonów H+ co OH–, tworzy się woda, a więc odczyn jest obojętny.
2 pkt – zastosowanie
poprawnej metody
obliczenia, i poprawne
wykonanie obliczeń, ale
błędna ocena
i jej uzasadnienie.
mr = 78,00 cm3 · 1,21 g · cm-3 = 94,38 g HNO3
ms = 35% · 94,38 g : 100% = 33,03 g HNO3
Ms = 1,01g · mol-1 + 14,01g · mol-1 + 3 · 16,00g · mol-1 = 63,02g · mol-1 HNO3
ns = 33,03 g : 63,02 g · mol-1 = 0,52 mola HNO3
ns = 2,00 mol · dm-3 · 0,25 dm3 · 2 = 1 mol KOH
ms = 35% · 94,38 g : 100% = 33,03 g HNO3
Ms = 1,01g · mol-1 + 14,01g · mol-1 + 3 · 16,00g · mol-1 = 63,02g · mol-1 HNO3
ns = 33,03 g : 63,02 g · mol-1 = 0,52 mola HNO3
ns = 2,00 mol · dm-3 · 0,25 dm3 · 2 = 1 mol KOH
Hipoteza nie była poprawna. Odczyn roztworu jest zasadowy, ponieważ w roztworze znajduje się więcej jonów OH– (pochodzących z dysocjacji nadmiaru zasady) niż jonów H+.
0 pkt – zastosowanie błędnej
metody obliczenia, (ocena
i jej uzasadnienie są zgodne
z wynikami obliczeń
zdającego, ale niezgodne
z opisem wyników
doświadczenia umieszczonym
w informacji do zadania).
KOH
V = 250 cm3 = 0,25 dm3
cm= 2 mol/dm3
n = 0,5 mola KOH
cm= 2 mol/dm3
n = 0,5 mola KOH
HNO3
V = 78 cm3 = 0,078 dm3
cp = 35%
cp = 35%
x = n = 0,26 mola HNO3
Hipoteza nie była poprawna. Odczyn roztworu jest kwasowy ponieważ znajduje się w nim więcej jonów H+ (pochodzących z dysocjacji nadmiaru kwasu) niż jonów OH–.
0 pkt – zastosowanie błędnej metody obliczenia (ocena i uzasadnienie są niezgodne z obliczeniami, mimo że są zgodne z opisem wyników doświadczenia umieszczonym w informacji do zadania).
schemat punktacji
3 pkt – poprawna metoda obliczeń, poprawne obliczenia oraz poprawna ocena i uzasadnienie.
2 pkt – poprawna metoda obliczeń, obliczenia z błędem rachunkowym oraz ocena spójna z obliczeniami i poprawne uzasadnienie.
2 pkt – poprawna metoda obliczeń, poprawne obliczenia oraz błędna ocena i uzasadnienie lub brak oceny.
1 pkt – poprawna metoda obliczeń, obliczenia z błędem rachunkowym, błędna ocena i uzasadnienie lub brak oceny.
0 pkt – brak odpowiedzi lub ocena bez obliczeń i uzasadnienia, lub ocena bez uzasadnienia niezgodna z obliczeniami, lub ocena z niepoprawnym uzasadnieniem.
2 pkt – poprawna metoda obliczeń, obliczenia z błędem rachunkowym oraz ocena spójna z obliczeniami i poprawne uzasadnienie.
2 pkt – poprawna metoda obliczeń, poprawne obliczenia oraz błędna ocena i uzasadnienie lub brak oceny.
1 pkt – poprawna metoda obliczeń, obliczenia z błędem rachunkowym, błędna ocena i uzasadnienie lub brak oceny.
0 pkt – brak odpowiedzi lub ocena bez obliczeń i uzasadnienia, lub ocena bez uzasadnienia niezgodna z obliczeniami, lub ocena z niepoprawnym uzasadnieniem.