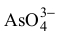Wskazówka:
Im większa wartość stałej dysocjacji kwasowej, tym większe stężenie danego jonu
powstającego w wyniku dysocjacji. Najwyższa jest wartość stałej dysocjacji Ka1 , więc
możemy stwierdzić, że największe jest stężenie jonów
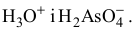
Najniższą wartość przyjmuje stała dysocjacji Ka3 , zatem stężenie jonu