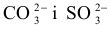Wskazówka:
Aby rozwiązać zadanie, należy zwrócić uwagę na to, że wszystkie użyte w doświadczeniu
substancje, które rozpuszczono w wodzie, są solami. Roztwory wodne wielu soli mają odczyn
inny niż woda, który jest obojętny. Zależy to od tego, z jakich wodorotlenków i kwasów sole
te powstały. Przyczyną zjawiska jest reakcja hydrolizy kationów lub anionów
wprowadzonych do wody w momencie rozpuszczania w niej soli. Hydrolizie ulegają kationy
pochodzące od słabych zasad, powodując zakwaszenie roztworu, i aniony pochodzące
od słabych kwasów, w czego wyniku roztwór uzyskuje odczyn słabo zasadowy. Kationy Na+
i Ca2+ pochodzą od mocnych zasad, więc są trwałe w środowisku wodnym, a kationy Fe2+ pochodzą od słabej zasady, będą zatem ulegać reakcji z wodą, powodując słabo kwasowy
odczyn roztworu. Aniony Cl– pochodzą od mocnego kwasu i nie reagują z wodą, natomiast
aniony