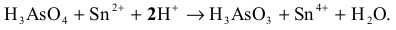Wskazówka:
W części b) wykorzystamy to, co zrobiliśmy w części a), pamiętając, że podstawą bilansu
równań reakcji redoks jest bilans elektronowy: liczba elektronów oddanych musi być równa
liczbie elektronów pobranych. W przypadku rozpatrywanej reakcji liczba ta wynosi 2, z czego
wynika, że stosunek liczby moli reduktora do utleniacza jest równy 1:1, a więc możemy
zsumować stronami równania procesów utleniania i redukcji, otrzymując następujący zapis:
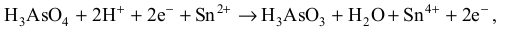
co pozwala nam uzupełnić współczynniki w podanym w zadaniu schemacie równania reakcji: