Odpowiedź:
Przykłady poprawnych odpowiedzi
Dane:
V = 50 cm3 = 0,050 dm3
mZnO = 243 mg = 0,243 gMZnO = 81 g · mol-1
Szukane:
cZn2+
Rozwiązanie:
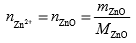
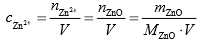
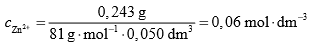
II sposób
1 mol Zn2+ --------- 81 g ZnO
x --------- 0,243 g ZnO
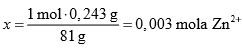
0,003 mola Zn2+ --------- 50 cm3=0,050 dm3 roztworu
y --------- 1 dm3 roztworu
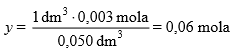
III sposób
Z równania reakcji
1 mol ZnS --------- 1 mol ZnO i MZnS = 97 g · mol-1 oraz MZnO = 81 g · mol-1
97 g ZnS --------- 81 g ZnO
x --------- 0,243 g ZnO
x = 0,291 g ZnS
MZnCl2 = 136 g · mol-1
136 g ZnCl2 --------- 97 g ZnS
y --------- 0,291 g
y = 0,408 g ZnCl2
136 g ZnCl2 --------- 1 mol
0,408 g --------- z
z = 3 · 10-3 mol i 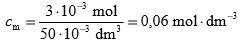
Odpowiedź: Stężenie molowe jonów cynku w badanym roztworze było równe 0,06 mol · dm-3.