N2 (g) + 3H2 (g) ⇄ 2NH3 (g)
ΔH = –92,4 kJ
Na położenie stanu równowagi tej reakcji wpływ mają temperatura i ciśnienie.
W poniższej tabeli przedstawiono równowagowe zawartości amoniaku (w procentach
objętościowych) w stechiometrycznej mieszaninie azotu i wodoru pod różnym ciśnieniem
i w różnych temperaturach.
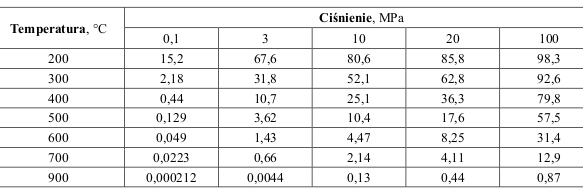
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004, s. 649.